在生命科学研究中,RNA干扰技术已成为基因功能研究的利器。而siRNA转染试剂作为递送siRNA进入细胞的关键工具,其性能将直接影响着实验成败。
各位科研小伙伴们,是否经历过以下“至暗时刻”:精心设计的siRNA,转染进去却“石沉大海”。RT-qPCR结果显示基因几乎没被敲低?明明镜下“荧光点点”,Western Blot条带却黑得发亮,仿佛转了个“寂寞”?
今天,为大家隆重介绍全村最靓的仔-siRNA转染试剂,它就像为RNAi实验量身打造的“黑科技”,助您轻松攻克实验难关!
01.为什么选择siRNA专用转染试剂?
传统观念认为,能转染质粒DNA的试剂就一定能转染siRNA,然而事实并非如此:
质粒DNA通常有数千碱基对,结构相对稳定。而siRNA大小通常为21-23bp,其作为核糖核苷酸极易被降解 。此外,两者的胞内作用机制完全不同:质粒DNA通过胞吞作用进入细胞,并从内涵体中逃逸出来进入细胞核才能实现基因的过表达,而siRNA由于极易降解则需要更高的内涵体逃逸效率,否则可能被困其中最终被溶酶体降解,无法释放到细胞质中与mRNA结合发挥基因沉默作用 。
因此,针对siRNA设计专用转染试剂从而实现“精准制导”是RNAi干扰转染实验的绝佳选择。
02.被隔壁实验室追问的ABclonal-siRNA转染试剂,转染界的何方魔丸?
产品亮点
1-基因沉默效率高:专为RNAi实验设计,精准制导基因沉默
2-极致低细胞毒性:可降解生物纳米材料,守护细胞健康状况
3-广谱细胞适用性:适用于多种类型细胞,硬核细胞不再“难啃”
4-操作简单快捷:只需孵育5 min,新手也能轻松拿捏
产品性能展示
细胞兼容广泛
使用ABclonal siRNA转染试剂转染小干扰RNA至多种贴壁/悬浮细胞,均可实现高效基因沉默。
基因沉默效率高
分别使用ABclonal、Vendor T RNAiMAX和Vendor YS siRNA转染试剂进行RNAi实验测评,结果表明:在同等实验条件下,RT-qPCR和Western blot结果显示,ABclonal的敲低效果与主流进口转染试剂Vendor T RNAiMAX基本相当,优于Vendor YS。
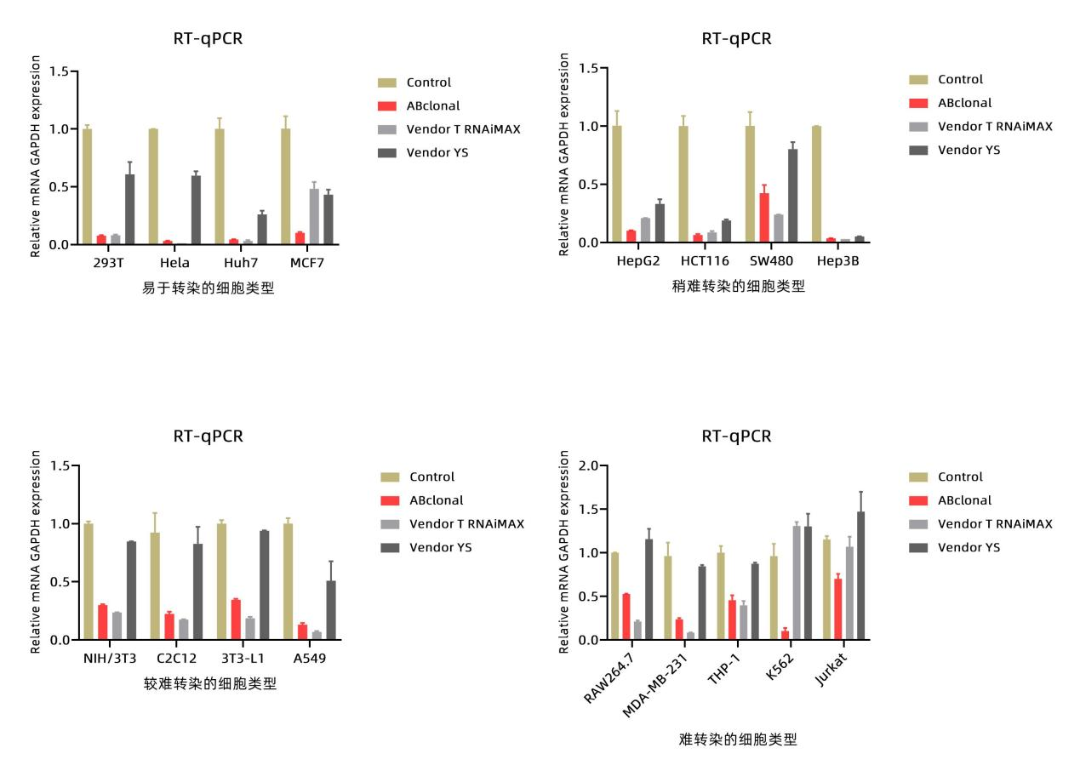
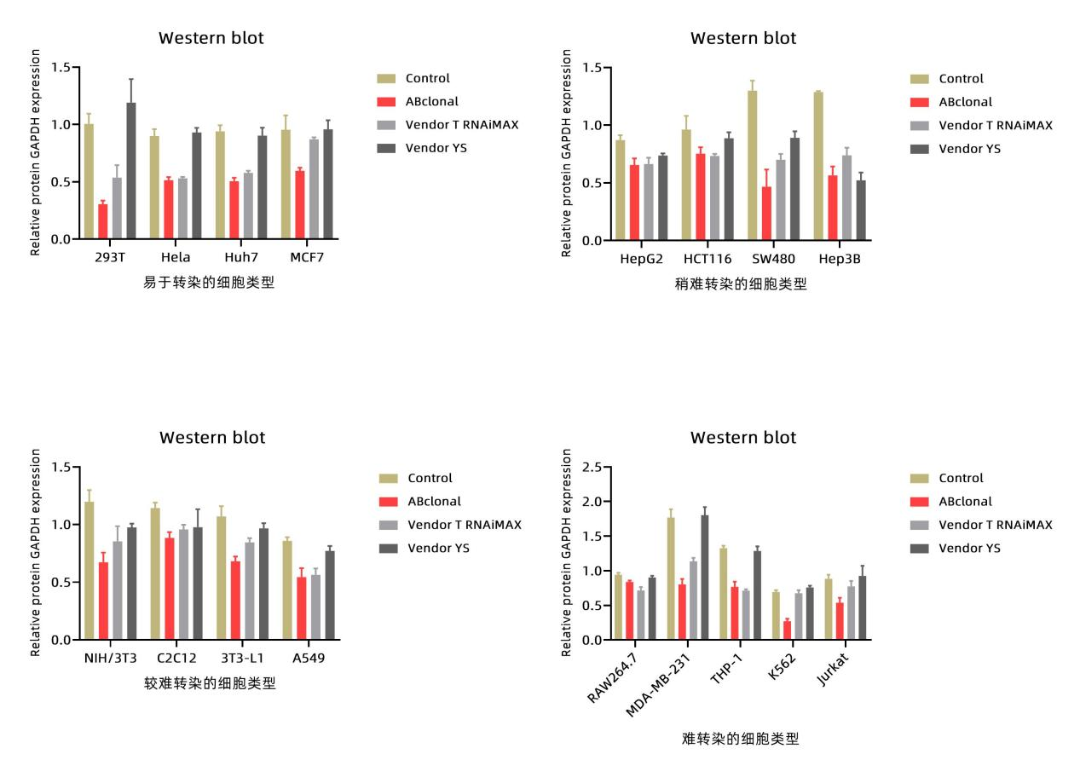
图1. 基因敲低测评结果(RT-qPCR/Western blot)
03.siRNA转染实验的流程
siRNA转染操作流程总览
siRNA转染操作步骤包括:细胞准备与接种、siRNA转染复合物的制备、转染复合物加入到细胞中。
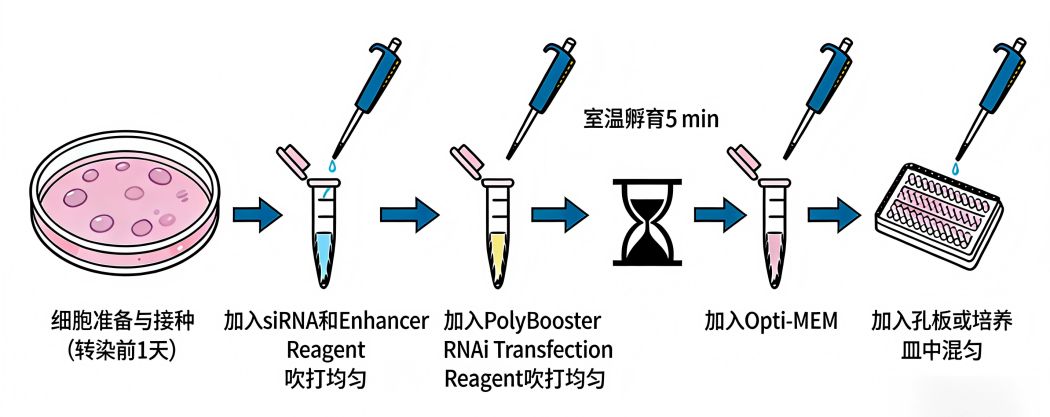 图2. siRNA转染实验操作流程总览(注:图片来源于网络)
siRNA转染实验全流程细节把控
1.细胞准备:
图2. siRNA转染实验操作流程总览(注:图片来源于网络)
siRNA转染实验全流程细节把控
1.细胞准备:
-
1-细胞状态:使用形态正常,细胞活率在90%以上的健康细胞,确保细胞没有被细菌、真菌或支原体污染。如果细胞是近期复苏的细胞,需要在转染前传代3~4次。
-
2-细胞密度:建议在转染前24 h接种细胞,贴壁细胞转染时的细胞密度一般在70%-90%。
-
3-细胞培养基:用于转染实验的细胞最好不要在完全培养基中添加抗生素,对于一些敏感细胞,抗生素的存在会引起细胞毒性。
2.转染复合物的制备:
-
1-siRNA-Enhancer Reagent:取适量的siRNA、Enhancer Reagent于微量离心管中,轻柔吹打混匀。
-
2-siRNA-Enhancer Reagent-转染试剂:取适量的PolyBooster RNAi Transfection Reagent加入到a步骤溶液中,轻柔吹打混匀,室温静置孵育5 min。
-
3-siRNA转染复合物的稀释:向b步骤溶液中加入适量的Opti-MEM,轻柔吹打混匀。
3.转染复合物加入到细胞中:
-
1-转染复合物滴加时需要逐滴加入,并及时充分混匀,避免培养基局部转染试剂浓度过高。
-
2-转染后8 h后可更换新鲜培养基。对于一些敏感细胞,换液处理可以降低细胞毒性。
4.实验结果的分析:
-
1-选择合适的分析方法。运用qPCR检测目的基因mRNA的表达情况,运用Western blot检测目的蛋白的表达情况。
-
2-合适的检测时间。mRNA水平的检测一般在转染后24~48 h,蛋白水平的检测一般在48~72 h。不同基因的半衰期不同,建议多设几个时间点进行检测,并根据实际情况合理调整检测时间。
04.产品订购信息
 05.相关产品推荐
05.相关产品推荐
 06.常见问题与解决方案
06.常见问题与解决方案
1-siRNA 转染与质粒DNA 转染的区别
2-转染的阳性对照组siRNA-FAM-NC,在显微镜下基本观察不到荧光信号或荧光信号微弱
FAM标记的荧光探针在转染之后会逐渐淬灭,因此最佳的观察时间一般在转染之后的 8 h 左右。同时,由于FAM的荧光信号较为微弱,使用荧光显微镜可能存在无法能有效观察到荧光信号的现象。
3-荧光对照组有荧光信号,但目的基因检测结果均无敲低效果
-
1-siRNA设计或靶点问题: siRNA本身无活性,或存在脱靶效应。建议使用至少2-3条针对同一个靶基因不同的siRNA序列。同时使用已验证过的阳性对照siRNA(如siRNA-GAPDH)来排除转染体系本身的问题。
-
2-siRNA质量问题:siRNA存在降解,或使用了未纯化/未修饰的廉价siRNA。建议进行严谨的预实验验证,并使用高质量的、经过修饰的siRNA以确保其稳定性和特异性。同时需要注意siRNA储存的条件和时间。
4-RT-qPCR结果显示基因表达水平敲低效果明显,Western blot结果显示蛋白表达水平基本没有下调效果
-
1-mRNA水平的检测一般在转染后24-48 h,蛋白水平的检测一般在转染后48-72 h。不同基因的半衰期不同,因此,建议多设几个时间点进行检测,根据实际情况合理调整检测时间。
-
2-目的蛋白半衰期:查找并确认检测的目的蛋白大致半衰期,如果半衰期较长,可能需要更长的沉默干扰时间才能检测到目的蛋白表达水平下调。
-
3-翻译效率反馈性升高:存在当细胞内某个关键蛋白表达量减少时,细胞内稳态调控机制会启动负反馈调节作用,将剩余少量mRNA更高效地翻译成相对应的蛋白。因此,如果无法延长实验时间(mRNA敲低效果只能维持几天时间),可以考虑尝试进行重复转染(在第一次转染后3-4天再次转染)来维持对细胞内相应mRNA水平的持续敲低。
-
4-蛋白稳定性补偿:存在当某种蛋白表达量减少时,为维持内环境稳态,细胞会启动抑制该蛋白的降解通路(如抑制其泛素化降解等),导致蛋白分子的半衰期变长。因此,建议可以尝试结合蛋白质合成抑制剂(如CHX等)进行干预处理,但这通常只适用于相关机制的研究,不适用于常规基因敲低实验。
-
5-样本制备问题:尽量使用同一批转染处理的细胞,或将总细胞裂解液分为两份:一份用于提取总细胞RNA,一份用于提取细胞总蛋白,确保两组数据来源完全一致。
-
6-抗体过载/信号饱和:显影曝光时间过长或蛋白上样量过大可能会导致wb条带信号达到饱和,导致目的条带微小差异被掩盖。可尝试将蛋白样品进行梯度稀释上样或缩短曝光时间,观察条带灰度值是否在线性范围内存在差异。







